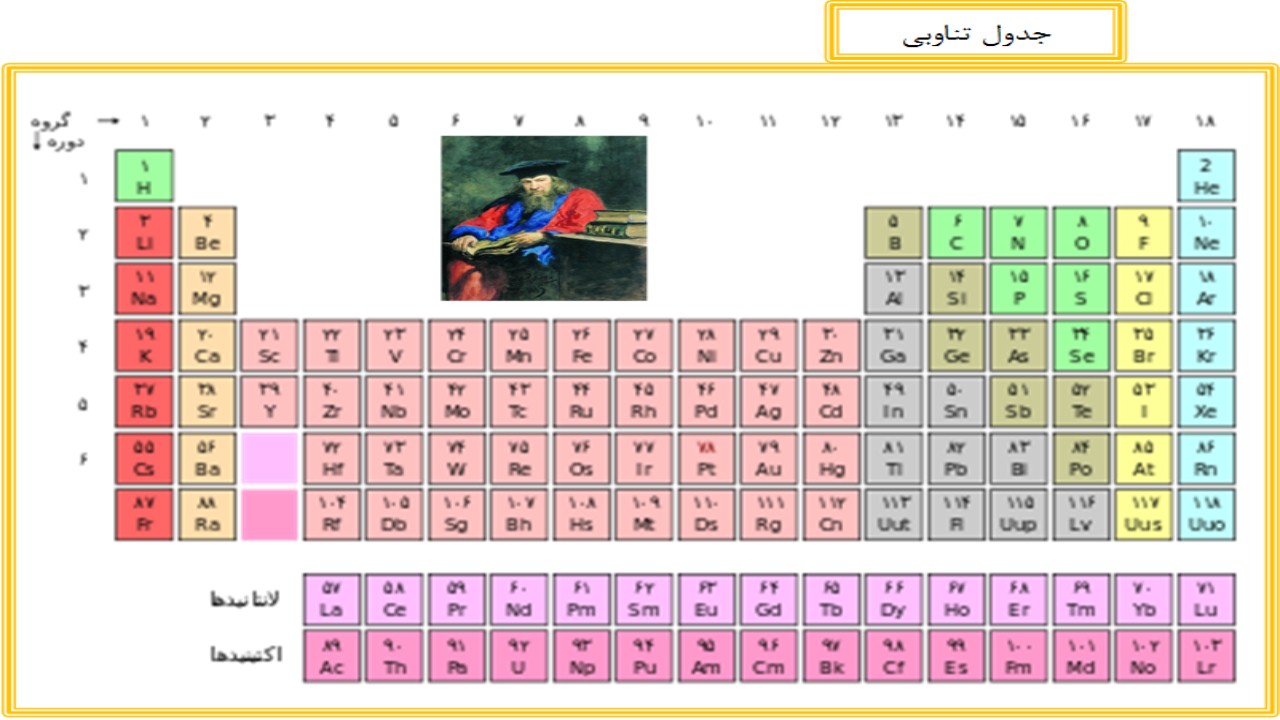
- هر عنصر به شیوه ای متفاوت با دیگر عناصر رفتار می کند و خواص آنها با هم متفاوت است امّا در عین حال شباهاتی نیز در چگونگی رفتار عناصر وجود دارد .
- عنصر هایی که آرایش الکترونی مدار بیرونی آنها یکسان است شبیه به هم رفتار می کنند . مانند لیتیم ، سدیم و پتاسیم و ... .
- جدول تناوبی 18 گروه دارد که در هر گروه عناصر با کوچکترین عدد اتمی در بالا و عناصری با بزرگترین عدد اتمی در پائین قرار می گیرد .
- در جدول تناوبی عناصر به چهار دستة زیر تقسیم می شوند :
1-فلز 2- نافلز 3- شبه فلز 4- گاز های نجیب
فلزات : فلزّات عناصری هستند که تمایل به از دست دادن الکترون دارند و یون مثبت می سازند. واکنش پذیرترین فلزّات در سمت چپ جدول تناوبی قرار دارند مانند سدیم و پتاسیم. عنصر های موجود در طبیعت فلزند.
نافلزات : نافلزّات عناصری هستند که تمایل به گرفتن الکترون دارند و یون منفی می سازند مانند هیدروژن، کربن، نیتروژن، اکسیژن، فلوئور، فسفر، گوگرد، کلر، سلنیم، ید و تمام گاز های نجیب .
شبه فلزّات : شبه فلزّات نیز خواصّی مابین فلزّات و نافلزّات دارند مانند : بور، سیلیسیم، ژرمانیم، آرسنیک، آنتیموان، تلوریم، پلونیم، استاتین .
گاز های نجیب : عناصر گروه هجدهم که الکترون های مدار آخرشان کامل است و واکنش ناپذیرند را گاز های نجیب تشکیل می دهند که شامل گاز های هلیم ، نئون ، آرگون ، کریپتون ، زنون و رادون می شوند .
کلمات کلیدی:
مخلوط و جداسازی مخلوط ها
تمام مواد موجود در طبیعت را به دو گروه بزرگ ماده مخلوط و ماده خالص طبقه بندی می کنند.
ادامه این دسته بندی را در نمودار زیر مشاهده کنید.
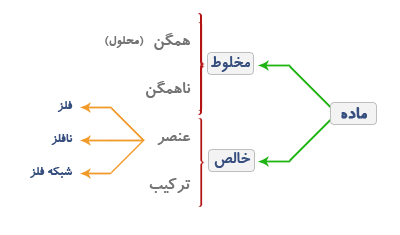
الف: ماده مخلوط
ماده ای است که از در هم آمیختن دو یا چند ماده حاصل می شود به شرطی که هر ماده ویژگی های خود را حفظ کند.
آب نمک، خاک باغچه ، سالاد، شربت خاک شیر، هوا ، شیشه، انواع آلیاژها و ... نمونه هایی از مخلوط هستند.


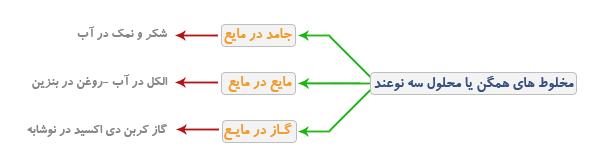

در محلول های جامد در مایع همیشه جزء مایع حلال و جزء دیگر حل شونده است.
در محلول های مایع در مایع جزئی که مقدارش بیشتر است حلال و جزء دیگر حل شونده است.


سالاد، آجیل، شربت خاکشیر، آب گل آلود، شربت معده و ... همگی مخلوط ناهمگن هستند.
ب) ماده خالص :
ماده ای است که تنها از یک جزء ساخته شده اند به عبارت دیگر ماده خالص ماده ای است که تنها از یک نوع عنصر و یا یک نوع ماده مرکب تشکیل شده است.
اکسیژن، گوگرد ، ئیدروژن و فسفر عنصر خالصند یعنی از مولکولهایی با اتمهای یکسان تشکیل شده اند و آب مقطر، کربن دی اکسید، الکل و نمک طعام مواد مرکب خالصند.
عنصر یا ماده ساده :
ماده ای است که از اتم های یکسان ساخته شده است.
فلز:
عناصری مانند آهن، مس، طلا، نقره، آلومینیوم و جیوه را فلز می گویند تقریبا همه این عناصر دارای ویژگی های زیر هستند.

نافلزها:
عناصری مانند کربن، گوگرد، فسفر، ید ، برم و ... را نافلز می گویند نافلزها دارای ویژگی های زیر هستند.

شبه فلز :
عناصری که خواص آنها از بین فلز و نافلز قرار می گیرد شبه فلز نامیده می شوند. عناصری مانند: سیلسیوم، آرسنیک، آنتیموان، تلوریم، ژرمانیوم جزء شبه فلز ها محسوب می شوند.
ترکیب:
ماده ای است که ذرات سازنده آن از دو یا چند نوع اتم متفاوت تشکیل شده است.
مولکول یک ماه مرکب ممکن است از دو ، سه و ... و یا تعداد بسیاری زیادی اتم تشیکل شده باشد.

ناخالصی:
ماده خالص در طبیعت کمیاب است و به همراه هر ماده مقداری مواد دیگر وجود دارد به این مواد همراه ناخالصی گفته می شود.
در بیشتر مواقع سعی می شود درجه خلوص مواد را بالا ببرند اما گاهی ناخالصی های همراه مواد سبب بهبود ویژگی ها و افزایش استحکام مواد می شود: مثلا با افزودن ناخالصی به فلزات آلیاژ یا همجوشه ساخته می شود که از نظر استحکام و دوام مطلوب تر است.
در جدول زیر با برخی از آلیاژها و کاربردآنها آشنا می شوید.
|
نوع آلیاژ |
فلزات تشکیل دهنده |
برخی کاربردها |
|
برنج |
مس+ روی |
چرخ دنده- ابزارهای علمی |
|
برنز |
مس+ قلع |
ابزار علمی |
|
مفرغ |
قلع+ سرب+ مس+ آشیموان |
لوازم آشپزخانه |
|
آمالگان |
جیوه + مس |
پرکردن دندان |
|
فولاد |
آهن+ کروم+ کربن |
تیرآهن- ماشین- ابزار |
|
نقره استرلنیگ |
نقره+ مس |
قاشق و چنگال |
انحلال پذیری :
اگر حل کردن شکر در آب را ادامه دهیم به جایی می رسیم که دیگر شکر در آب حل نمی شود به چنین محلولی سیرشده می گوییم.
اگر حلال را گرم کنیم مقدار بیشتری از حل شونده را در خود حل خواهد کرد به این محلول فوق اشباع یا فراسیر شده می گویند بنابراین افزایش دما سبب افزایش انحلال پذیری می شود.
اگر چنین محلول هایی سرد شوند مقداری از ماده حل شده بصورت بلور از محلول جدا می شود یعنی قابلیت حل شدن با کاهش دما کم می شود.
بطور کلی انحلال پذیری یعنی بیشترین مقدار ماده ای که در یک دمای معینی می توانند در 100 گرم آب حل شود.
انحلال پذیری گازها: گازها هم مانند جامدات و مایعات در آب حل می شوند، ماهیها از اکسیژن محلول در آب استفاده می کنند. کربن دی اکسیدکربن محلول در نوشابه از ایجاد تغییرات شیمیایی نامطلوب در نوشابه جلوگیری می کند.
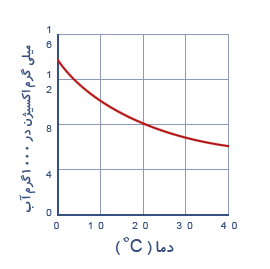
البته بر خلاف آنچه در بالا گفته شد انحلال پذیری گازها با افزایش دما کاهش می یابند نمودار مقابل این مطلب را نشان می دهد.
همانطورکه از نمودار بر می آید هر چه آب گرمتر شود از مقدار اکسیژن محلول در آن کاسته می شود.
جداسازی اجزاء یک مخلوط:
در بیشتر مواقع لازم است که اجزاء یک مخلوط را از هم جدا کنیم. برای تهیه آب شیرین نمک و سایر املاح را از آب جدا می کنند . فراورده های نفتی هم بصورت مخلوط با یکدیگر تحت عنوان نفت خام یافت می شوند.
زمانی می توان اجزاء یک مخلوط را از هم جدا کرد که اجزاء حداقل در یک ویژگی با هم اختلاف داشته باشند.
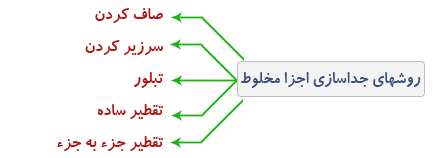
الف) صاف کردن:
از این روش هنگامی استفاده می شود که اجزاء مخلوط از نظر اندازه ذرات با هم تفاوت داشته باشند. الک کردن آرد، جداکردن شن و ماسه از یکدیگر، جداکردن تفاله از چای نمونه هایی از صاف کردن هستند.
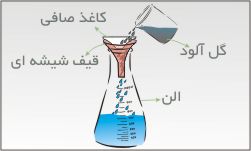
ب) سرریز کردن:
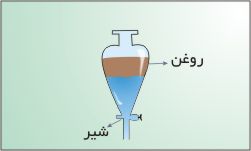
هنگامی از این روش استفاده می شود که یک جزء از جزء دیگر سبک تر باشد. اگر مخلوط آب روغن بی حرکت بماند چون روغن از آب سبک تر است بر روی آب قرار می گرید و می توان با سر ریز کردن و یا با استفاده از وسیله مقابل که قیف جدا کننده یا قیف دکانتور نامیده می شود آنها را از هم جدا کرد.
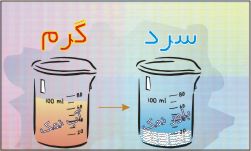
ج) تبلور:
از روش تبلور برای جدا کردن جزء جامد از مایع استفاده می شود . اگر مخلوط جامد در مایعی مانند آب نمک را سرد کنیم از آنجا که انحلال پذیری با کاهش دما کم می شود مقداری از حل شونده بصورت بلور در ته ظرف ته نشین می شود.
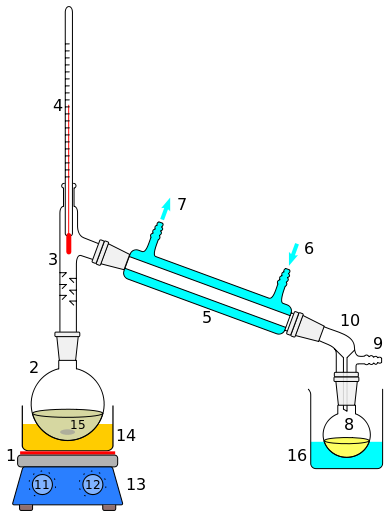
د)تقطیر ساده:
از تقطیر ساده برای جداکردن دو جزء مایع مخلوط که نقطه جوش متفاوت دارند استفاده می شود مثل الکل از آب .
برای مشاهدة توضیحات دربارة شماره های روی تصویر ماوس را روی شکل ثابت نگه دارید .
ه) تقطیر جزء به جزء:
از این روش برای جدا کردن اجزاء مخلوط چند مایع که نقطه جوش متفاوت دارند استفاده می شود اجزاء نفت خام را به همین روش از هم جدا می کنند. به این ترتیب که نفت خام را تا 400 درجه سانتیگراد حرارت می دهند تا بسیاری از اجزاء آن بجوش آیند و بصورت بخار در آیند. نفت خام حرارت داده شده را به قسمت پایین دستگاهی به نام برج تقطیر می فرستند بخارات حاصل هنگام صعود از دستگاه به سینی های نصب شده برخورد کرده و بر اساس تفاوت نقطه جوش به مایع تبدیل و از هم جدا می شوند.
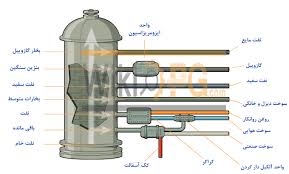
تقطیر جزء به جزء نفت خام
کلمات کلیدی:
