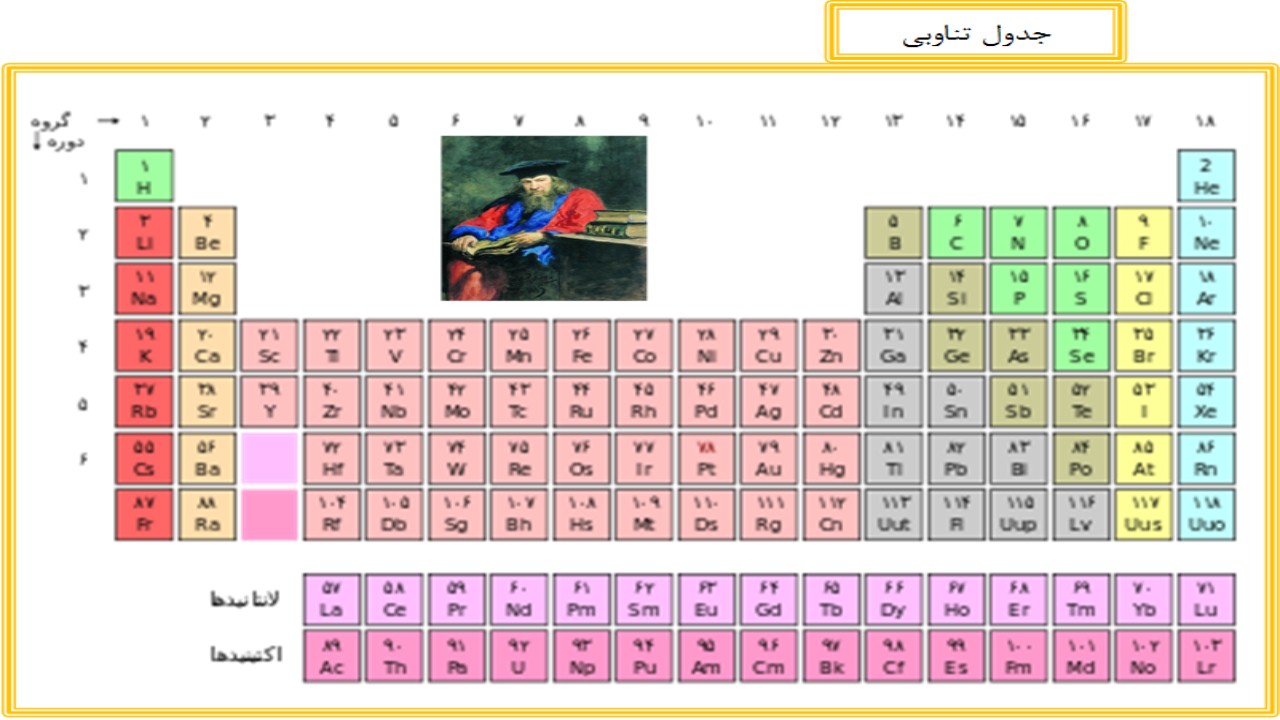
1-فلز 2- نافلز 3- شبه فلز 4- گاز های نجیب
فلزات : فلزّات عناصری هستند که تمایل به از دست دادن الکترون دارند و یون مثبت می سازند. واکنش پذیرترین فلزّات در سمت چپ جدول تناوبی قرار دارند مانند سدیم و پتاسیم. عنصر های موجود در طبیعت فلزند.
نافلزات : نافلزّات عناصری هستند که تمایل به گرفتن الکترون دارند و یون منفی می سازند مانند هیدروژن، کربن، نیتروژن، اکسیژن، فلوئور، فسفر، گوگرد، کلر، سلنیم، ید و تمام گاز های نجیب .
شبه فلزّات : شبه فلزّات نیز خواصّی مابین فلزّات و نافلزّات دارند مانند : بور، سیلیسیم، ژرمانیم، آرسنیک، آنتیموان، تلوریم، پلونیم، استاتین .
گاز های نجیب : عناصر گروه هجدهم که الکترون های مدار آخرشان کامل است و واکنش ناپذیرند را گاز های نجیب تشکیل می دهند که شامل گاز های هلیم ، نئون ، آرگون ، کریپتون ، زنون و رادون می شوند .
کلمات کلیدی: